来源:网络资源 2022-12-07 20:26:54
一、物态变化的含义
1.物态变化
物质由一种状态变为另一种状态的过程
2.性质
首先利用分子动理论从微观意义上解释物态变化的本质
2.1物质是由大量的分子组成的
2.2分子永不停息地做着无规则的运动
2.3分子之间是有间隔的,并且存在相互作用力:引力和斥力
二、凝固知识点
1.凝固定义:
物质从液态变成固态的过程,需要放热。
2.凝固现象:
①“滴水成冰”②“铜水”浇入模子铸成铜件
3.凝固规律:
①晶体在凝固过程中,要不断地放热,但温度保持在熔点不变。
②非晶体在凝固过程中,要不断地放热,且温度不断降低。
4.晶体凝固必要条件:
温度达到凝固点、不断放热。
5.凝固放热:
①北方冬天的菜窖里,通常要放几桶水。(利用水凝固时放热,防止菜冻坏)
②炼钢厂,“钢水”冷却变成钢,车间人员很易中暑。(钢水凝固放出大量的热)
6.同一晶体的熔点和凝固点相同;
7.注意:
7.1物质熔化和凝固所用时间不一定相同,这与具体条件有关;
7.2热量只能从温度高的物体传给温度低的物体,发生热传递的条件是:物体之间存在温度差;
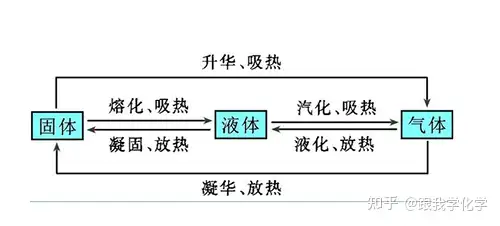
三、熔化知识点
1.熔化定义:
物质从固态变成液态的过程需要吸热。
2.熔化现象:
①春天“冰雪消融”
②炼钢炉中将铁化成“铁水”
3.熔化规律:
①晶体在熔化过程中,要不断地吸热,但温度保持在熔点不变。
②非晶体在熔化过程中,要不断地吸热,且温度不断升高。
4.晶体熔化必要条件:
温度达到熔点、不断吸热。
5.有关晶体熔点(凝固点)知识:
①萘的熔点为80.5℃。
当温度为790℃时,萘为固态。
当温度为81℃时,萘为液态。
当温度为80.50℃时,萘是固态、液态或固、液共存状态都有可能。
②下过雪后,为了加快雪熔化,常用洒水车在路上洒盐水。(降低雪的熔点)
③在北方,冬天温度常低于-39℃,因此测气温采用酒精温度计而不用水银温度计。
6.熔化吸热的事例:
①夏天,在饭菜的上面放冰块可防止饭菜变馊。(冰熔化吸热,冷空气下沉)
②化雪的天气有时比下雪时还冷。(雪熔化吸热)
③鲜鱼保鲜,用0℃的冰比0℃的水效果好。(冰熔化吸热)
④“温室效应”使极地冰川吸热熔化,引起海平面上升。
7.晶体和非晶体的区分标准是:
晶体有固定熔点,熔化时温度不变继续吸热;而非晶体没有固定的熔点,熔化时温度升高,继续吸热。
常见的晶体有:冰、食盐、萘、各种金属、海波、石英等
常见的非晶体有:松香、玻璃、蜡、沥青等
8.影响熔点、凝固点的因素
①压强。平常所说的物质的熔点,通常是指一个大气压时的情况。对于大多数物质,熔化过程是体积变大的过程,当压强增大时,这些物质的熔点升高;对于像铋、锑、冰来说,熔化过程是体积变小的过程,当压强增大时,这些物质的熔点降低。
②物质中混有杂质。纯净水和海水的熔点有很大的差异。
四、凝华
1.凝华定义:
物质从气态变成固态的过程,需要放热。
2.凝华现象:
①霜和雪的形成(水蒸气遇冷凝华而成)
②冬天看到树上的“雾凇”
③冬天,外界温度极低,窗户内侧可看见“冰花”(室内水蒸气凝华)
五、升华
1.升华定义:
物质从固态变成气态的过程,需要吸热。
2.升华现象:
①加热碘,可以看到有紫红色的碘蒸气出现。
②衣柜中防虫用的樟脑片,会慢慢变小,最后不见了。
③冬天,湿衣服放在户外会结冰,但最后也会晾干。(冰升华成水蒸气)
3.升华吸热:
①干冰可用来冷藏物品。(干冰是固态二氧化碳,升华成气态时,吸收大量的热)
六、液化
1.液化定义:
物质从气态变成液态的过程,需要放热。
2.液化现象:
①水开后,壶嘴看见“白气”(壶中汽化出水蒸气,遇到冷空气液化成雾状小水珠)
②夏天自来水管和水缸上会“出汗”。(空气中的水蒸气遇冷液化成水珠)
3.液化的方法分为:
降低温度、压缩体积两种方法
3.1降低温度(遇冷、放热)液化:
①雾与露的形成(空气中水蒸气遇冷液化成雾状小水珠;附在尘埃浮在空中,形成“雾”;附在草木,聚成“露”)
②冬天,嘴里呼出“白气”。夏天,冰棍周围冒“白气”。(水蒸气遇冷液化成雾状小水珠)
③冬天,窗户内侧常看见模糊的“水气”。(屋内水蒸气遇到冷玻璃液化成小水珠)
④牙医在为病人检查牙齿时,将检查用的小镜子在酒精灯上稍微烤一下,然后放入口腔中。(防止口腔内的水蒸气遇冷液化成小水珠附在镜面上)
3.2压缩体积液化:
①在常温下,将石油气压缩放入钢瓶中,以液态石油气的形式保存。
②“长征”火箭的燃料和助燃剂分别是:压缩成的“液态氢”和“液态氧”。
③打火机中,常用压缩后的液态“丁烷”作为燃料。
4.液化放热:
①北方的冬天,在室内暖气管道中通以灼热的水蒸气来取暖,最后在管道另一头回收到的是水。(水蒸气液化成水放出大量热)
②100℃的水蒸气比100℃的水更容易烫伤人体。(100℃的水蒸气液化成100℃的水要放热)
七、汽化
1.汽化:
物质从液态变成气态的过程,需要吸热。
2.汽化现象分为:
沸腾、蒸发,两种形式都要吸热。
八、沸腾和蒸发的区别
1.沸腾:
1.1沸腾现象:例-水沸腾,有大量的气泡上升,变大,到水面破裂,释放出水蒸气。
1.2沸腾规律:液体在沸腾时,要不断地吸热,但温度保持在沸点不变。
1.3液体沸腾必要条件:
温度达到沸点、不断吸热。
1.4有关沸点知识:
①液态氧的沸点是-183℃,固态氧的熔点是-218℃。-182℃时,氧为气态。
-184℃时,氧为液态。-219℃时,氧为固态。-183℃氧是液态、气态或气液共存都可以。
②可用纸锅将水烧至沸腾。(水沸腾时,保持在100℃不变,低于纸的着火点)
③装有酒精的塑料袋挤瘪(排尽空气)后,放入80℃以上的水中,塑料袋变鼓了。
(酒精汽化成了蒸气。酒精沸点为78℃,高于78℃时为气态)
2.蒸发:
2.1蒸发现象:
①湿衣服放在户外,很快就会干
②教室洒过水后,水很快就干了
2.2蒸发吸热,有致冷作用:
①刚从水中出来,感觉特别冷。(风加快了身上水的蒸发,蒸发吸热)
②一杯40℃的酒精,敞口不断蒸发,留在杯中的酒精温度低于40℃。(蒸发要向周围环境和液体自身吸热。)
③在室内,将一支温度计从酒精中抽出,示数会先下降再升高。(酒精蒸发吸热,使温度计中液体温度下降,蒸发结束后温度回升到室温)
欢迎使用手机、平板等移动设备访问中考网,2023中考一路陪伴同行!>>点击查看