������ǻ�ѧ���һ�������ݣ�Ҳ���п�������֮�أ�����ʽ���ǿ����ij��͡�������ϸ���ܽ�����һר����ص�֪ʶ������㻹���κ����ʵĻ���һ��Ҫ��ϸ�Ķ���
һ���ἰ���ͨ��
��Ķ��壬����ʱ���ɵ�������ȫ������H+�������������Ӻ�������ӹ��ɡ�
1.Ũ���ᡢŨ������������ʡ����ԡ���;
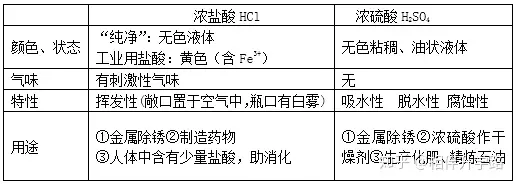
2.���ͨ�ԣ��� �� HCl �� �� H2SO4
��ʹ��ɫʯ����Һ��죬ʹ��ɫ��̪��Һ����ɫ��
����+��→��+����
Zn+2HCl=ZnCl2+H2↑
Zn+ H2SO4 =ZnSO4+H2↑
����������+��→��+ˮ
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
��+��→��+ˮ
NaOH+HCl=NaCl+ H2O
Cu(OH)2+H2SO4= CuSO4+2H2O
��+��→��һ����+��һ����
AgNO3+HCl=AgCl↓+HNO3
BaCl2+H2SO4=BaSO4↓ +2HCl
ע�⣺(1)��‘����+��→��+����’�У���ͨ��ָ����ϡ�����ϡ���ᣬ������Ũ��������ᡣ
��ΪŨ��������ᶼ��ǿ�����ԣ��������Ӧʱ��������������������ˮ��
(2)ͨ����������ķ�Ӧ������������˳�����
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
���������ǿ�����������˳���У�����λ��Խ��ǰ�����Խǿ����ӦԽ���ң�����ʱ��Խ�̡�
(3)Ũ���������ˮ�ԣ�ͨ��������Ϊ�������
���ỹ������ˮ�ԣ�����Ƥ�����·��к�ǿ�ĸ�ʴ�ԡ�
ϡ��Ũ����ʱһ��Ҫ��Ũ������������������ע��ˮ������Ͻ������в��ɰ�ˮ����Ũ����������ˮע��Ũ�����ˮ���ܶȽ�С���ḡ���������棬�ܽ�ʱ�ų����Ȼ�ʹˮ���̷��ڣ�ʹ����Һ���Ĵ��ɽ����������¹ʡ�
��������ͨ��
���壺����ʱ���ɵ�������ȫ����OH-���ӡ������ɽ�������(��笠�����)�����������ӹ��ɡ�
1.�������ơ��������Ƶ��������ʡ���;
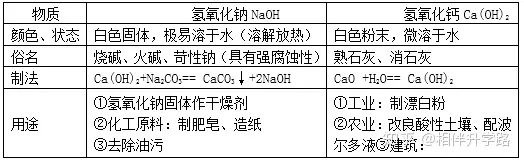
2.���ͨ��
��ʹ��ɫʯ����Һ������ʹ��ɫ��̪��Һ��졣
��������ʹ��ɫʯ����Һ��������ɫ��̪��Һ��졣
��������ʹ��ɫʯ����Һ��������ɫ��̪��Һ��졣
����������+��→��+ˮ
2NaOH+CO2=Na2CO3+H2O Ca(OH)2+CO2=CaCO3↓+H2O
��+��→��+ˮ
NaOH+HCl=NaCl+H2O
Ca(OH)2+H2SO4= CaSO4+2H2O
��+��→��һ����+��һ�ּ�
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
ע�⣺(1)ֻ�п����Լ���ܸ�һЩ�ǽ������������Ӧ����Щ�ǽ���������������������������������������ˮ����ˮ���������ᡣ
(2)�κͼӦʱ���������߶��ǿ��ܵģ���������֮һ�dz�������Ӧ���ܽ��С�
(3)��д���ijЩ���������ﷴӦ�Ļ�ѧ����ʽ
�������෴Ӧ��ѧ����ʽ����д��ͬѧ�е������ѣ�Ϊ�ˣ�����д���ǽ����������ˮ��Ӧ�����ɺ�����Ļ�ѧ����ʽ�����Ժ�����ͼ�������ɷ�д���������ʽ�ϲ���һ����ѧ����ʽ��
����������������
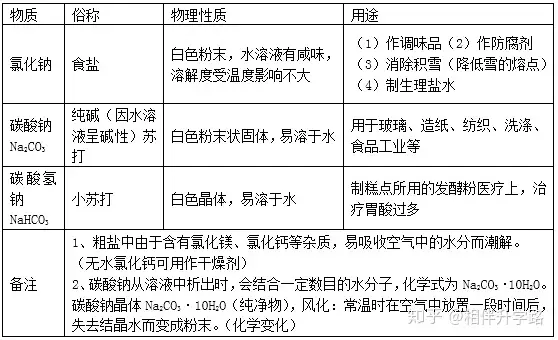
1.��������
���壺�ܽ������������(��NH4+)��������ӵĻ����
ע����ʱ���β���ָʳ�Σ�ʳ�ε���Ҫ�ɷ���NaCl��
2.�����ᴿ
ȥ�����������ʣ��õ��ľ����л������Ȼ�þ���Ȼ��Ƶȿ��������ʡ�
(1)ʵ�鲽�裺�ܽ⡢���ˡ�����

(2)ʵ������
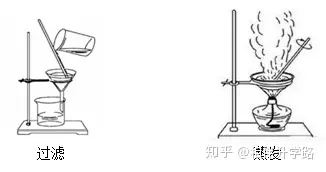
ע�⣺
�� �������ǿ���ֱ�Ӽ��ȵ�������Һ��������ܳ���������2/3.
�� �ܽ�ʱ�ò��������裬Ŀ���Ǽӿ��ܽ⡣
�� ����ʱ�ò��������裬��ֹ�ֲ��¶ȹ������Һ�ηɽ�
�� ���������г��ֽ϶����ʱֹͣ���ȣ���������ʹ��Һ���ɣ����ܽ���Һ��ȫ���ɲ�ͣ����ֹ���ȡ�
3.�εĻ�ѧ����
����Һ+����→�Ψ@+�����@
CuSO4+Zn= ZnSO4+Cu
��+��→�Ψ@+ ��@
BaCl2+H2SO4=BaSO4↓ +2HCl
����Һ+����Һ→�Ψ@+��@
3NaOH+FeCl3=3NaCl+Fe(OH)3 ↓
����Һ+����Һ→�Ψ@+�Ψ@
AgNO3+NaCl=AgCl↓+NaNO3
ע�⣺�ڽ����˳����У�ֻ������ǰ��Ľ������ܰ����ں���Ľ��������ǵ�����Һ���û���������K��Ca��Na���ֽ���������Һ�ķ�Ӧ���⣬���ﲻҪ��
�ġ����ֽⷴӦ������η�Ӧ
1.���ֽⷴӦ
���ֽⷴӦ�Ķ����ǣ������ֻ�����������ɷ֣������������ֻ�����ķ�Ӧ��
ͨʽ��AB+CD=AD+CB
2.����������
������������Һ����������ӣ�������������г�������������ų�����ˮ���ɣ����ֽⷴӦ�����Է�����
3.�������������ﷴӦ�����ڸ��ֽⷴӦ
�塢����ᡢ��ε��ܽ���
�ᡢ��ε��ܽ��Լ���ھ���
���а����ء��ơ������ƿ���
������������Σ� ȫ�����������Ρ�
�����β��ܱ���Ǧ;
�Ȼ��ﲻ�����ǹ��� ̼���γ�������ܣ��������ܡ�
���������������ӵļ���
1.Cl-���ӵļ���
(�ֱ�Ϊʵ����� ʵ������ ʵ����� ��ѧ����ʽ)
ȡ������Ʒ���Թ��У��μ�AgNO3��Һ��ϡHNO3
�в�����ϡ����İ�ɫ��������
��Ʒ����Cl-
AgNO3+KCl=AgCl↓+KNO3
2.SO42-���ӵļ���
ȡ������Ʒ���Թ��У��μ�Ba(NO3)2��Һ��ϡHNO3
�в�����ϡ����İ�ɫ��������
��Ʒ����SO42-
Ba(NO3)2+H2SO4=BaSO4↓+2HNO3
3. CO32-���ӵļ���
ȡ������Ʒ���Թ��У��μ�ϡHCl,�����ɵ�����ͨ�����ʯ��ˮ
����ɫ�������ɣ�������ʹ����ʯ��ˮ�����
��Ʒ����CO32-
K2CO3+2HCl=2KCl+ CO2↑+H2O
CO2+Ca(OH)2= CaCO3↓+ H2O
4.����NH4+
ȡ�����������ڽྻ���Թ��У���������NaOH��Һ�����ȣ���ʹʪ�ĺ�ɫʯ����ֽ�����ɫ�����������
5.����ϡ�����ϡ����
�ֱ�ȡ��������Һ������֧�ྻ���Թ��У������뼸��BaCl2��Һ���а�ɫ����������ԭ��Һ��ϡ���ᣬ�����������ԭ��Һ��ϡ���ᡣ
�ߡ�����Ԫ�غ�ԭ���ŵĻ��ϼ�
(����)һ�������������þ��п���������Ĺ衢�嵪�ס�
(����)��һ�ۣ������ȡ��塢��;
�����ۣ�������
(�ɱ�����)��һ��ͭ����������������̼��������
ԭ���ŵĻ��ϼۣ�
��һ�ۣ�������(OH)�������(NO3)�������(ClO3)���������(MnO4);
�����ۣ������(SO4)��̼���(CO3)���������(SO3)�������(MnO4);
�����ۣ������(PO4); ��һ�ۣ�笠�(NH4)��
�ˡ�����׳ơ���Ҫ�ɷֺͻ�ѧʽ
��ʯ��—— CaO
��ʯ��——Ca(OH)2
ʯ��ʯ������ʯ—— CaCO3
ʳ��——NaCl
���ռ������—— NaOH
����մ�——Na2CO3
С�մ�—— NaHCO3
���⡢������——Fe2O3
������—— Fe3O4
���ʯ��ʯī—— C
�ɱ�——CO2
��—— H2O
��Ȼ��(����)——CH4
�ƾ�(�Ҵ�)—— C2H5OH
����(����)——CH3COOH
�š��������ʵ���ɫ
��ɫ�Ĺ���——Cu��Fe2O3 ��P(����)
��ɫ�Ĺ���——C��CuO��Fe3O4��FeO��MnO2
��ɫ�Ĺ���——KClO3��P2O5��P(����)��CuSO4(��ˮ����ͭ)��KCl��NaCl��
����ɫ�Ĺ���——KMnO4
��ɫ�Ĺ���—— S
��ɫ�Ĺ���——CuSO4•5H2O
��ɫ����——Cu(OH)2
���ɫ����——Fe(OH)3
������������İ�ɫ����——BaSO4��AgCl
�����Ტ�ų�ʹ����ʯ��ˮ����ǵ�����İ�ɫ����——BaCO3��CaCO3
�����ᵫ����������İ�ɫ����——Mg(OH)2��Al(OH)3�Ȳ����Լ�ij���
��ɫ����Һ—— CuSO4��CuCl2��Cu(NO3)2�Ⱥ�Cu2+��Һ
dz��ɫ����Һ——FeSO4��FeCl2�Ⱥ�Fe2+��Һ
��ɫ����Һ——FeCl3��Fe2(SO4)3��Fe(NO3)3�Ⱥ�Fe3+��Һ
�������з�Ӧ����ʽ��
1.������ͭ��ϡ���ᷴӦ�� Cu(OH)2 + 2HCl = CuCl2 + 2H2O ��ɫ������ʧ
2.������ͭ��ϡ���ᷴӦ�� Cu(OH)2 + H2SO4 = CuSO4 + 2H2O �����ɫ��Һ
3.�������Ƹ�����ͭ��Һ��Ӧ��2NaOH + CuSO4 = Na2SO4 + Cu(OH)2 ↓ ����ɫ��������
4.�������Ƹ��Ȼ�����Һ��Ӧ��3NaOH + FeCl3 = Fe(OH)3↓ +3NaCl �к��ɫ��������
�ж���Һ�������
��ָʾ������Һ������——��pH����ʾ��
�������ѡ��
1.Ũ����ɸ��
��������(�磺CO2��SO2��SO3��NO2��HCl��)
��������(�磺H2��O2��N2��CO)
�����ܸ����������(�磺NH3)
2.�������ƹ��塢��ʯ�ҡ���ʯ�ҿɸ��
��������(�磺NH3)
��������(�磺H2��O2��N2��CO)
�����ܸ�����������(�磺CO2��SO2��SO3��NO2��HCl)
3.��ˮ����ͭ������ˮ�ɰ�ɫ����ɫ���ɼ���ˮ�Ĵ��ڣ�������ˮ������
���� ��ӭʹ���ֻ���ƽ����ƶ��豸�����п�����2024�п�һ·���ͬ�У�>>����鿴














