来源:网络资源 2022-12-10 21:39:37
-1-
“七嘴八舌”说考情
■ 陕西中考说:必考。多以溶解度曲线结合实物操作图或者表格形式命题,每年考查的形式均不相同。近4 年均在18题题位考查。
■ 山西中考说:仅2017年未考。除2014年(溶解度表)、2011年(1条曲线+实物操作图)外,其余均是考查2种未知物质的溶解度曲线。仅2016年在实验探究题中考查,其余均在填空题中考查。
■ 河南中考说:必考。 除2015年(溶解度表)、2010年(一种未知物质的溶解度曲线),其余均是考查两种未知物质的溶解度曲线。
■ 河北中考说:仅2010年未考。常在选择题中以溶解度曲线的形式进行考查,偶尔也会以文字描述或溶解度表格的形式进行考查。
■ 云南中考说:必考。在选择题、填空与简答中均有涉及。多以三条或两条曲线的形式考查,但是偶尔也会以一条曲线的形式考查相关知识。
■ 安徽中考说:必考。考查形式多样,考查一条曲线时,曲线走势有“只上升和先升后降”型;考查两条曲线时,曲线走势有“2升”、“1升1降”和“2降”型。
■ 江西中考说:必考。 曲线的形式包括“1 升 1 降”、“2升”、“2升1降”等。也会以曲线结合表格形式,或单独以操作图的形式考查。
-2-
说来说去还得练
1. (推荐云南、安徽、江西、河北) 甲、乙两固体物质的溶解度曲线如图所示,下列说法错误的是( )
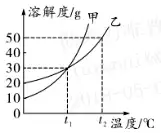
甲、乙两物质的溶解度均随温度的升高而增大
t1℃时,甲物质的溶解度和乙物质的溶解度相等
t1℃时,甲物质和乙物质的饱和溶液的溶质质量分数均为30%
t2℃时,乙物质的饱和溶液降温后会有晶体析出
2. (推荐河南、河北) a、b两物质在不同温度时的溶解度如表所示,根据表中信息,判断下列说法不正确的是 ( )
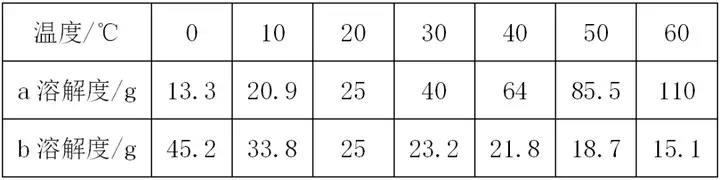
20℃时,向100 g水中加入25 g固体a,所得溶液质量是125 g
b物质的溶解度随温度的升高而减小
50℃时,100 g b物质的饱和溶液中有
18.7 g b物质
将30℃时,a、b两物质的饱和溶液同时降温至20℃,所得溶液的溶质质量分数的大小关系是a>b
3. (推荐云南、安徽) 如图是一种固体物质(不含结晶水)的溶解度曲线。 下列说法错误的是( )
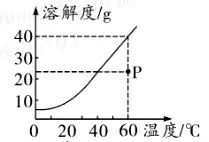
60℃时该物质的溶解度为40 g
该物质的溶解度随温度的升高而减小
P点表示60℃时该物质的不饱和溶液
可以通过降温结晶的方法提纯该物质
4. (推荐江西) A、B、C三种物质的溶解度曲线如图所示,请回答下列问题。
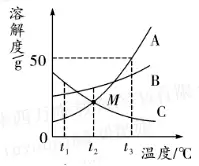
(1)t1℃时, A、B、C三种物质的溶解度由大到小的顺序是______。
(2)t3℃时把50g A 放入50g水中得到A的______(填“饱和”或“不饱和”)溶液,此时溶液中溶质和溶液的质量比为______。
(3)将t3℃ 时,A、B、C三种物质的饱和溶液降温至t2℃,所得溶液的溶质质量分数的大小关系是______。
5. (推荐陕西) 如图是硝酸钾和氯化钠在不同温度时的溶解度曲线,下表是两种物质在部分温度时的溶解度数据。
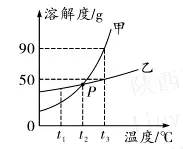
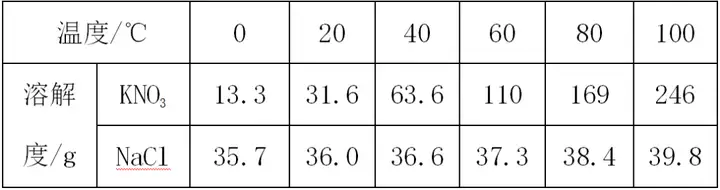
(1)根据溶解度表格可知,溶解度曲线图中甲表示_______的溶解度曲线。
(2)若甲物质中混有少量的乙物质,提纯甲物质最好采取的方法是____(填“ 降温结晶”或“ 蒸发结晶”)。
(3)将t1℃ 的甲、乙两物质的饱和溶液(均无固体物质剩余) 升温到t2℃ 时,所得甲物质溶液的溶质质量分数____(填“大于”、“小于”或“等于”)乙物质溶液的溶质质量分数。
6. (推荐江西) t1℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100 g水的烧杯中,充分搅拌后现象如图1,加热至t2℃时现象如图2。甲、乙、丙三种物质的溶解度曲线如图3。 请结合图示回答下列问题:
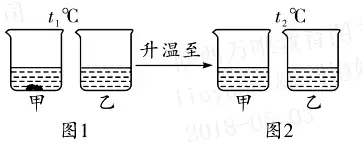
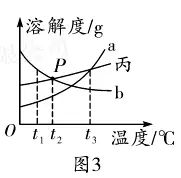
(1)分析图1和图2中的现象,判断符合甲物质的溶解度曲线是图3中的____(选填“a”或“b”);图中P点表示的含义是______。
(2)t1℃时,甲、乙、丙的饱和溶液的溶质质量分数从小到大的顺序是_____。
(3)t3℃时,将等质量的甲、乙、丙的饱和溶液降温到t1℃,一定有晶体析出的是 _____ 。
7. (推荐陕西) 下表是 a、b两物质在不同温度时的溶解度,分析表中数据,回答问题。
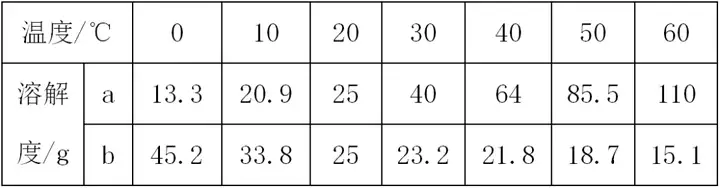
(1)20℃时,向 50 g水中加入25 g的固体a,所得溶液质量是_____g。
(2)将30℃时,a、b两物质的饱和溶液同时升温至40℃,所得溶液的溶质质量分数的大小关系是a____b(填“>”、“<”或“=”)。
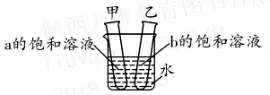
(3)如图所示,现有20℃时等质量的a、b两物质的饱和溶液,向烧杯的水中加入一定量的硝酸铵,溶解后甲试管内出现的现象是_____;乙试管内的溶液是_____(填“饱和”或“不饱和”)溶液。
【答案】
1.C 2.C 3.B
4.(1)C>B>A (2)饱和 1:3
(3)B>A>C
5.(1)硝酸钾(或KNO3) (2)降温结晶
(3)小于
6.(1)a t2℃时,乙和丙的溶解度相等
(2)甲 < 丙 < 乙
(3)甲和丙
7.(1)62.5 (2)>
(3)有晶体析出 不饱和
-3-
专家秘招赶紧看
一、溶解度曲线
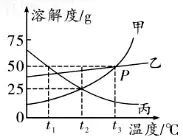
要点1:溶解度随温度的变化趋势
✪
如:甲、乙的溶解度均随温度的升高而增大,丙的溶解度随温度的升高而减小 。
■ 方法指导:看曲线的坡度及走向,从左到右看曲线的走势是向上、向下还是平缓。向上表示随温度升高溶解度增大(如甲、乙);平缓表示随温度升高溶解度增大的趋势不显著(如乙);向下表示随温度升高溶解度减小(如丙)。
要点2: 溶解度曲线交点的含义
✪
如:P点表示:t3℃时,甲、乙的溶解度相等,均为50 g 。
■ 方法指导:曲线交点表示该温度时,两种物质的溶解度相等,此时两种物质饱和溶液的溶质质量分数也相同。描述两条溶解度曲线交点所表示的意义时要指明温度。
要点3:溶解度大小的判断与比较
✪
如:t1℃时,三种物质的溶解度由大到小的顺为:丙>乙>甲 。
■ 方法指导:物质溶解度大小的比较离不开温度。过该温度对应的点作垂直于横轴的直线,看直线对应的交点的纵坐标:①该纵坐标为此温度下对应物质的溶解度。②针对两种或两种以上物质溶解度大小的比较,纵坐标越大,溶解度越大。
要点4:饱和溶液与不饱和溶液的判断及相互转化
✪
如:①t1℃时,将25 g甲物质加入到100 g水中,恰好形成甲的饱和溶液。②甲的饱和溶液升温后变成不饱和溶液。
■ 方法指导:
在一定温度下:

饱和溶液与不饱和溶液的转化:
①溶解度随温度的升高而增大,则

②溶解度随温度的升高而减小,则

✪ 要点5: 溶液溶质质量分数的计算与比较
如:t1℃时,将40 g丙加入到100 g水中,充分溶解,所得溶液的溶质质量分数为28.6%;t2℃时,甲的饱和溶液的溶质质量分数为20% 。
■ 方法指导:计算公式需谨记:
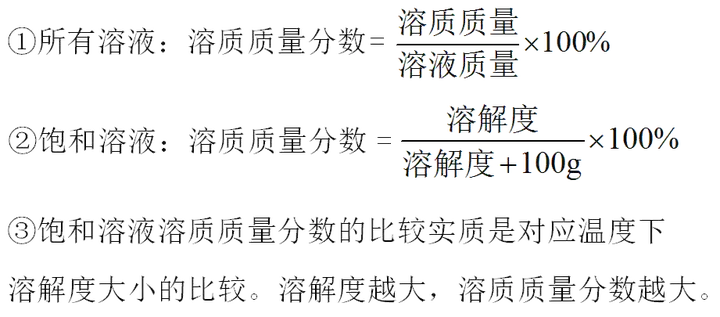
要点6:判断物质结晶的方法
✪

要点7: 温度改变时,溶液中各种量的变化情况
✪
如:t3℃时,将相同质量的甲、乙、丙的饱和溶液同时降温到t1℃,则下列说法正确的是(C )
A. 溶质质量分数:乙<丙
B. 溶剂质量:甲>乙
C. 溶质质量:乙>丙
D. 溶液质量:甲>丙
■ 方法指导:饱和溶液温度变化时:
(1)物质的溶解度随温度的升高而增大(即曲线为上升型)。
① 若将饱和溶液降低温度,由于析出晶体,溶液中溶质质量减小,溶剂质量不变,溶液质量减小,因此溶质质量分数变小。
② 若将饱和溶液升高温度,饱和溶液变为不饱和溶液,溶液中溶质、溶剂质量均不变,因此溶质质量分数也不变。
(2)物质的溶解度随温度升高而减小(即曲线为下降型)。改变温度时,溶液中溶质、溶剂、溶液的质量,溶质质量分数变化情况与上述分析相反。
二、溶解度曲线
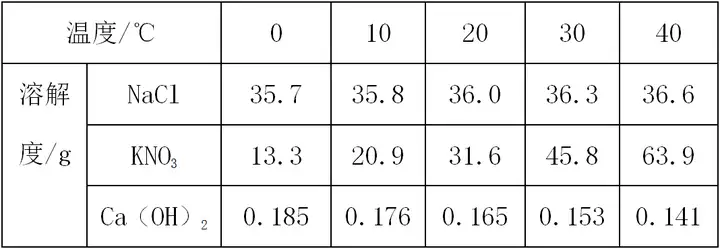
要点1:从表中直接读取信息
✪
(1)同一物质,不同温度下的溶解度。
如氯化钠在10℃时溶解度为35.8g,在30℃时溶解度为36.3g。
(2)不同物质,在同一温度下的溶解度。
如20℃时,氯化钠的溶解度为36.0 g,硝酸钾的溶解度为31.6g,氢氧化钙的溶解度为0.165 g。
(3)根据不同温度下溶解度的变化情况,判断物质的溶解度随温度的变化趋势。 如氯化钠的溶解度变化趋势为随温度升高,溶解度增大,但是幅度较小;硝酸钾的溶解度变化趋势为随温度升高增长幅度较大;氢氧化钙的溶解度变化趋势为随温度增大而减小 。(仅变化趋势、不做数据对比)
要点2:溶解度表的应用
✪
以表格数据形式考查两种物质(如NaCl和KNO3)溶解度相等的温度范围为20℃~ 30℃ 。
■ 方法指导:根据溶解度表,通过对比两种物质的溶解度,20℃以前,NaCl的溶解度大于KNO3,30℃以后,NaCl的溶解度小于KNO3,则NaCl和KNO3 溶解度相等的温度范围一定在20℃~ 30℃之间。
欢迎使用手机、平板等移动设备访问中考网,2023中考一路陪伴同行!>>点击查看